Tal y como vimos en el tema anterior, en el caso de los gases existe una relación entre la presión «p», el volumen «V», la temperatura «T» y la masa «m» o cantidad de moles. Recordemos que el número de moles «n» se obtiene de la expresión:
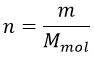
, siendo «Mmol» la masa molar de las moléculas del compuesto en cuestión. Partiendo de esto, podemos hacer una relación entre el volumen extensivo «V» y el intensivo «v» a través del número de moles:
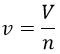

Si trazamos para el mismo gas la función «p v / T» frente a «p» para distintos valores de «T», observamos que cuando la presión tiende a 0:
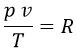
, siendo «R» una constante independiente de la temperatura. Despejando:
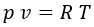
, y sustituyendo el volumen intensivo:
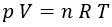
, que sería la ecuación del gas ideal, donde:
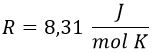
 Si ahora trazamos la gráfica de «p» frente a «v» para distintas temperaturas, las hipérbolas obtenidas serán denominadas isotermas, y tenderán a infinito mientras descienda la presión, disminuyendo hacia 0 cuando esta aumenta, ya que «p» y «v» son inversamente proporcionales:
Si ahora trazamos la gráfica de «p» frente a «v» para distintas temperaturas, las hipérbolas obtenidas serán denominadas isotermas, y tenderán a infinito mientras descienda la presión, disminuyendo hacia 0 cuando esta aumenta, ya que «p» y «v» son inversamente proporcionales:
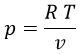
Si obtenemos una mezcla de «N» gases ideales inertes de composiciones distintas «ni», la ecuación se cumple para todos ellos en conjunto, pues obtenemos que:
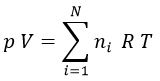
La presión parcial de cada uno de ellos será:
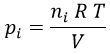
, mientras que:
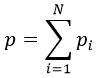
Además:
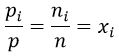
, siendo «xi» un coeficiente particular para cada gas en la mezcla.
Energía Interna de un Gas Ideal. Ley de Joule:
Supongamos un sitema adiabático (que no intercambie calor con el exterior), dividido en dos recintos: uno vacío y el otro ocupado por un gas. Si dejamos al gas ocupar todo el recinto, al no haber intercambio de energía con ningún sistema no vacío, el trabajo y el calor son nulos, por lo que la energía inerna no aumenta, según el Primer Principio de la Termodinámica:
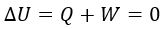
Así pues, la energía interna solo es función de la temperatura, porque la presión y el volumen no la alteran.
Intentemos en la gráfica adjunta calcular la variación de la energía entre el punto «i» y el punto «f».

Como la energía del gas es una función de estado, será independiente del proceso seguido, y podremos calcular su aumento parcialmente yendo primero del punto «i» al punto «a» por una isoterma, que por la Ley de Joule no variará su energía, y después avanzar desde «a» hasta «f» por una isocora:
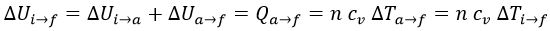
Es decir, el aumento de energía en un proceso isocorico depende del calor y el trabajo a volumen constante, siendo el segundo nulo según vimos en el tema antrerior, y el primero igual al calor específico, que depende del aumento de temperatura.
Un caso similar obtenemos si queremos calcular la entalpía, que desde «i» hasta «b» se define como:
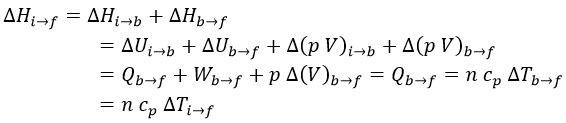
Como en una isoterma la energía interna y el producto «p v» son constantes, todos los términos se anulan mutuamente, y ésta toma el valor del calor específico a presión constante entre «b» y «f».
Ley de Mayer:
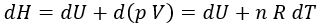
Si sustituimos en ambos miembros, obtenemos:
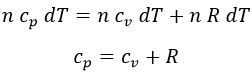
«Cp > Cv» siempre se cumple, y su diferencia es «R».
Para gases monoatómicos (helio, neón…):
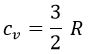
Para gases diatómicos (oxígeno, nitrógeno…):
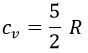
Transformaciones Adiabáticas de un Gas Ideal. Fórmula de Reech:
Dado que en un proceso adiabático no hay calor, se cumple siempre que:
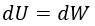
, y obtenemos la igualdad:
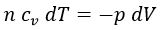
, de donde:
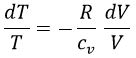
Si consideramos el coeficiente adiabático:
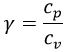
, que vale 5 / 3 para los gases monoatómicos y 7 / 5 para los gases diatómicos. Podemos obtener:
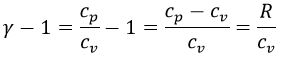
De aquí, si sustituimos e integramos en la ecuación anterior:
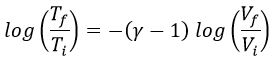
, y de donde:
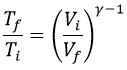
, o lo que es lo mismo:
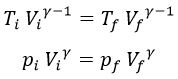
Pendiente de la Isoterma y de la Adiabática:
 Si representamos ambas curvas en la misma gráfica, y analizamos sus ecuaciones: isoterma:
Si representamos ambas curvas en la misma gráfica, y analizamos sus ecuaciones: isoterma:
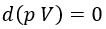
; adiabática:
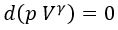
, y posteriormente las derivamos, obtenemos sus pendientes.
En la isoterma:
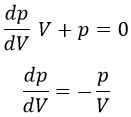
En la adiabática:
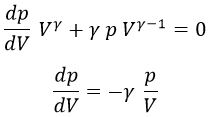
La pendiente de la adiabática es «γ» veces más inclinada.


necesito mas informacion concreta porfavor..!! algo como ..menos complicado..pero completo..y bien definido
hola como están, bueno tendré una exposición acerca de procesos reversibles, vaporización reversible de un liquido, expansión isotérmica reversible de gases ideales y energía interna del gas ideal. lo que busco es que necesito información de como hacer captar a mis compañeros esos temas, con ejemplos y unos conceptos claros y bien comprensivos, quisiera que me apoyen con la información necesaria, se los agradecería mucho.
Atte: Edher tueros yace