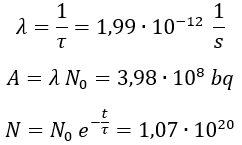7. FENÓMENOS CUÁNTICOS
7.1. La estructura atómica
7.2. El principio de incertidumbre
Mecánica cuántica.
Como vimos en el capítulo anterior, a principios del siglo XX el modelo atómico de Bohr había conseguido dar una cierta estructura matemática a la estructura del átomo de hidrógeno imponiendo que el momento angular de los electrones debía de estar cuantizado, y solo podía modificarse en múltiplos de la constante de Planck.
Sin embargo, muchos científicos pensaron que esa propiedad debía de ser una consecuencia de un axioma más general y no un principio básico de la naturaleza. Einstein intentó justificar que los electrones no pudiesen caer sobre el núcleo atómico apelando a la constante cosmológica como fuente de estabilidad, pero a día de hoy sabemos que no hay ninguna relación entre ambas cosas.
A principios de los años veinte, sin embargo, un enfoque completamente innovador apareció para poner en jaque todo cuanto se conocía sobre la naturaleza. El físico Werner Heisenberg había estado probando modificaciones de la teoría de Hamilton y concluido que se podía reproducir la estructura atómica con la consideración de que las coordenadas de un sistema físico no conmutaban con sus momentos asociados. De este modo, no sería lo mismo multiplicar la posición por el momento lineal que multiplicar el momento lineal por la posición. La idea, denominada mecánica cuántica, resultaba desagradable, pero los resultados eran concluyentes, siendo el más asombroso de ellos el principio de incertidumbre.
En esencia, este principio decía que el error al medir la coordenada dx de una partícula, multiplicado por el error al medir su momento asociado dpx tenía que dar siempre un resultado positivo:
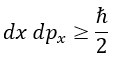
Siendo así las cosas, resultaría imposible conocer la posición de una partícula con una precisión absoluta, y además cuanto menor fuese el error de dicha medición más grande sería el error al medir su momento lineal. El mismo resultado es extrapolable a intentar medir el ángulo de giro y el momento angular a la vez, y a intentar medir el tiempo y la energía.
El principal éxito del principio de esta nueva propuesta fue dar un nuevo enfoque a la estructura del átomo. Aplicando las fórmulas de Bohr, el de hidrógeno debía tener un radio y una energía de:

Ahora bien, la energía de la órbita es, como sabemos, opuesta a la energía rotacional, de modo que podemos establecer la relación:

Consideremos ahora el siguiente supuesto: toda la energía del electrón es prácticamente la mínima que tiene que tener para que no se incumpla el principio de incertidumbre. La posición del electrón la conocemos con la precisión del radio de Bohr, con lo que el error en su momento debe de ser aproximadamente:
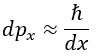
Y este error mínimo que debe haber en el momento lineal se traduce en un error mínimo en la energía rotacional de la forma:
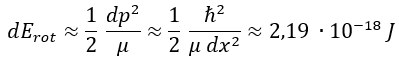
Que coincide exactamente con la energía de Bohr. Es necesario comprender la relevancia de lo que ha sucedido aquí: hemos podido determinar la energía del átomo de hidrógeno conociendo únicamente su radio y la masa del electrón, ignorando por completo tanto su carga como la del protón en el centro. En otras palabras, hemos resuelto una órbita electrostática sin tener en cuenta ningún concepto electrostático. La ecuación final es fácil ver que tiene que dar el resultado correcto porque coincide con la fórmula de la energía rotacional según el momento angular:
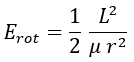
Parecía, en suma, que a pequeñas escalas de la naturaleza, el requisito impuesto por el principio de incertidumbre era suficiente para predecir algunas propiedades físicas esenciales. Además, una conclusión directa es que cuanto más intentemos encerrar una partícula mayor será su energía cinética y, por tanto, mayor será fuerza con la que se oponga.
Principio de incertidumbre.
Heisenberg sentó, con su principio, una forma de distinguir los sistemas donde era necesario aplicar la mecánica cuántica para trabajar de aquellos en los que esta podía ser completamente ignorada. De este modo, en nuestro día a día la incertidumbre cuántica no nos parece muy importante, pero al reducir nuestras escalas de observación se vuelve imprescindible.
Pero había algo anti intuitivo en todo ello. ¿Cómo podía ser correcta esa desigualdad matemática? ¿Por qué debía de suponer una barrera infranqueable a nuestra capacidad de observación? Intentando contestar a esta pregunta, Heisenberg puso como ejemplo el hecho de que siempre que intentamos analizar algún movimiento necesitamos ver el cuerpo: tanto dónde está como en qué instante está. El hecho de ver, a su vez, involucra la necesidad de que el cuerpo en cuestión interactúe con fotones. Al bombardear con un fotón una mesa, por ejemplo, difícilmente conseguiremos que el choque provoque un desplazamiento de la misma, pero si lo que queremos observar es una partícula elemental.
Siendo este el caso, el error en la posición de un electrón que queramos observar vendrá dado por la longitud de onda del fotón con el que lo intentemos detectar, y esto nos llevará a la irremediable conclusión de que cuanto más queramos precisar en la posición del electrón reduciendo la longitud de onda, mayor será la energía con la que lo golpearemos. A su vez, al ser mayor la energía del golpe, esta desviará más la trayectoria del electrón, con lo que perderemos la información sobre su momento lineal. En el caso contrario, si reducimos la longitud de onda del fotón para intentar no desviarlo mucho y conocer su momento lineal, perderemos precisión en su posición.
Esta consideración de que los fotones solo «ven bien» cosas del tamaño de su longitud de onda está muy relacionada con las propiedades de las ondas electromagnéticas a gran escala. Por ejemplo, el motivo por el que las ondas de radio pueden atravesar paredes de casas es porque su longitud de onda es de varios metros o incluso kilómetros, y ello les permite ignorar obstáculos cuya longitud sea inferior. Por el contrario, rayos ultravioleta, cuya longitud de onda característica es menor que el tamaño de muchas moléculas, está condenada a chocar con ellas en la atmósfera mientras intenta llegar hasta nosotros.
Onda de Schrödinger.
Poco tiempo después de que Heisenberg publicase sus fundamentos de la mecánica cuántica, pero antes de que publicase su principio de incertidumbre, el físico Erwin Schrödinger apostó a que había otra forma de describir los fenómenos cuánticos mucho más intuitiva basada en ondas, y obtuvo así su famosa ecuación de Schrödinger, la cual establecía que toda partícula cuántica tenía asociada una onda con la que se podía predecir su comportamiento. Esta idea estaba relacionada con la noción de dualidad onda-corpúsculo planteada por el físico Louis de Broglie. Si bien las partículas se comportaban esencialmente como corpúsculos, seguía teniendo sentido para ciertos procesos asignarles una longitud de onda y una frecuencia, y parecía que deberíamos aprender a convivir con ambas naturalezas. En efecto, Schrödinger no tardó en demostrar que ambos modelos, la mecánica cuántica de Heisenberg y su función de onda, debían reproducir siempre los mismos resultados, dando pie así la primera unificación entre dos teorías cuánticas.
Max Born, al leer sobre la teoría de Schrödinger y preguntarse acerca qué representaban dichas ondas, propuso considerar que en esencia describían la probabilidad de encontrar a la partícula en cada lugar del espacio. Así, aquellos lugares donde la función de onda fuese nula serían lugares donde la partícula no podría encontrarse en ningún caso. La ecuación de Schrödinger era, por tanto, un método de calcular probabilidades, y dichas probabilidades no serían reducibles a leyes físicas más fundamentales.
Copenhague.
La cuestión acerca de cómo interpretar la mecánica cuántica llegó hasta la conferencia Solvay de 1927, un evento donde se reunían los principales físicos de Europa cada año para discutir sus avances conjuntamente. Allí, Bohr y Einstein tuvieron posturas muy encontradas al respecto.
Einstein y Schrödinger, entre otros, defendían que la naturaleza no podía ser aleatoria, y que la ecuación de onda debía de ser únicamente una aproximación estadística. El hecho de que no fuésemos capaces de predecir lo que sucedería con una partícula antes de observarla tenía que ser una consecuencia de nuestra ignorancia, y no de que no hubiese explicación alguna. Esta era la postura determinista.
En el bando contrario, Bohr y la inmensa mayoría de asistentes defendían que la mecánica cuántica suponía el fin del determinismo y había que renunciar a intentar encontrar explicaciones más fundamentales. En este sentido, Bohr llegó a desarrollar una filosofía un tanto peculiar acerca de la realidad, según la cual el electrón, su posición y su momento no existían hasta que no eran observados, y únicamente al interactuar con este se volvía real.
Schrödinger intentó ridiculizar dicho punto de vista haciendo una analogía con un gato encerrado en una caja. Si este era encerrado junto con una partícula que podía, aleatoriamente, matarle o no, la tesis de Bohr implicaría que el gato no estaría ni vivo ni muerto hasta que abriésemos la caja para interactuar con él.
Siguiendo con las críticas, Einstein tampoco se quedó atrás, y junto con Rosen y Boris Podolsky publicó en 1935 una crítica a la mecánica cuántica como modelo de la realidad fundamentada en dos pilares:
- Un modelo de la realidad en el que esta no existe no puede ser un modelo completo acerca de la naturaleza.
- La tesis del colapso de la función de onda para dar lugar a magnitudes reales podía involucrar fantasmales acciones a distancia.
La segunda crítica estaba relacionada con las consecuencias de llevar los postulados de Bohr hasta el límite. Si teníamos una función de onda que involucrase a dos partículas diferentes, y las separábamos a cualquier distancia, la mecánica cuántica predecía que al medir una y volverse algunos de sus parámetros reales, también quedaban instantáneamente determinados los valores de la otra. Si esto realmente sucedía así, podría involucrar una transmisión de información más rápida que la luz, lo cual contradecía todo el esfuerzo llevado a cabo por Maxwell y por él mismo para establecer que nada podía viajar más rápido que la luz en el vacío.
Durante la segunda mitad del siglo XX, el físico John Bell convertiría esta crítica en una predicción, al mostrar experimentalmente que dos partículas cuánticas que formasen parte de un mismo estado podían influirse de forma instantánea a cualquier distancia. Desde entonces el concepto de entrelazamiento a distancia pasó a ser una realidad, y la idea de que nada podía propagarse más rápido que la velocidad de la luz tuvo que ser puesta en entredicho.
El descubrimiento de Bell fue recibido con los brazos abiertos por parte de la comunidad de físicos seguidores de la tesis de Bohr, quienes se vieron legitimados para decir que no tenía sentido intentar predecir el movimiento exacto de las partículas sino, a lo sumo, sus posibles estados globales. En el bloque sobre física actual volveremos a tratar este tema.
Efecto túnel.
A finales del siglo XIX, el físico Henri Bécquerel descubrió que algunos átomos, sin ninguna influencia externa, emitían radiación en forma de partículas. Este descubrimiento le llevó a clasificar como materiales radiactivos aquellos que tenían esta extraña propiedad, y a indagar en el fenómeno, un interés que inspiraría posteriormente a Marie Curie y a Pierre Curie.
Todos ellos trabajaron con el concepto de actividad de los materiales radiactivos, definiendo como tal a la cantidad de partículas que radiaban en un determinado segundo. En el SI, la actividad se mide en becquerelios (bq).
Una propiedad muy curiosa de los fenómenos radiactivos, a día de hoy sin resolver, era que no existía ninguna forma de predecir en qué instante emitirían radiación. Era como si el instante en el que un átomo concreto fuese a desprenderse de parte de su energía fuese completamente aleatorio, y además la probabilidad de que lo hiciese ni siquiera aumentaba con el tiempo. Este fenómeno, por supuesto, fue muy bien acogido por las ideas de la mecánica cuántica.
Gamow fue el primero, poco después de la conferencia Solvay, en darse cuenta de que el principio de incertidumbre de Heisenberg era suficiente para explicarlo. Podía pensarse en un núcleo radiactivo, como punto de partida, como la unión de un núcleo estable y partículas extra. Debido a las fuerzas nucleares de cohesión, las partículas extra no podrían escaparse, ya que la energía potencial que ello requeriría sería muy superior a la suya. Sin embargo, a cierta distancia del núcleo, la energía potencial decaería de nuevo y sería incluso menor.
Se produce entonces una situación complicada de minimización: tanto a la parte del núcleo que es estable como a las partículas extra les interesa más separarse para reducir su energía potencial, pero para ello necesitan más energía potencial de la que disponen. Afortunadamente, el principio de incertidumbre de Heisenberg estaba ahí para ayudar:
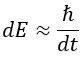
Dado que la energía tiene que tener cierta indeterminación, siendo esta inversamente proporcional al error en la medición del tiempo, las partículas podrían escaparse del núcleo siempre y cuando lo hiciesen en menos tiempo que el que el relacionado con la energía extra que necesitasen. Como este fenómeno vendría dictaminado por el principio de incertidumbre, y este era intrínsecamente impredecible, la conclusión era que no habría nunca una forma de predecir el instante en el que un núcleo radiactivo emitiría radiación. Además, tal y como se había observado, no sería más probable que el núcleo radiase porque hubiese pasado el tiempo. A este mecanismo de la naturaleza para atravesar barreras de potencial se le denominó efecto túnel, ya que en cierto modo el principio de incertidumbre habilita un túnel de atajo para llegar hasta la escapatoria.
Si denominamos vida media de un núcleo al tiempo τ que transcurre en promedio hasta que emite radiación, la probabilidad λ de que se desintegre en un segundo, su actividad, es de:

A esta probabilidad por unidad de tiempo se la denomina constante de desintegración, y si tenemos N núcleos idénticos, la cantidad de ellos que se desintegrarán en un segundo, es decir, la actividad total, es de:
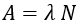
Y dado que la actividad mide la cantidad de núcleos que se desintegran en un segundo, la siguiente ecuación representa cuál es la derivada temporal de la cantidad de núcleos:

Y si la derivada de la cantidad de núcleos es proporcional a sí misma, debe cumplirse que, en promedio:

Donde N0 es la cantidad de núcleos inicial de la muestra.
La vida media de un núcleo radiactivo es de 15900 años. Calcula:
a) Su constante de desintegración.
b) La actividad de una muestra de 2*10^20 núcleos.
c) La cantidad de núcleos que quedarán, en promedio, tras 10000 años.
Todos los apartados se calculan con sus fórmulas:
Además de los datos anteriores, resulta útil saber despejar el tiempo que tardarán en quedar una cierta cantidad de núcleos:

A partir de aquí, se define como semivida t1/2 de una muestra al tiempo que tardará, en promedio, en reducirse a la mitad:

Dado que el logaritmo está en base natural, y el logaritmo natural de 2 es menor que 1, la semivida siempre es menor que la vida media. Es decir, el núcleo promedio emite radiación después de que lo hayan hecho el 50% de los núcleos, lo cual nos da una idea de la enorme cantidad de núcleos que tardan en desintegrarse más de lo esperable.
Veamos, para concluir con esta sección, un último ejemplo muy clásico relacionado con la datación de momias.
Cuando un ser humano está vivo, existen en su cuerpo la misma cantidad de átomos de carbono con 6 neutrones, más conocidos como carbono-12, que carbonos con 8 neutrones, conocidos como carbono-14. Al morir, el carbono-12 permanece estable, pero el carbono-14 comienza a desintegrarse liberando radiación, de modo que se va reduciendo con el paso del tiempo. Para saber cuánto tiempo ha transcurrido desde que una persona ha muerto, por tanto, basta con comparar la cantidad de carbono-14 que queda en su cuerpo en comparación con el carbono-12. Sabiendo que la vida media del carbono-14 es de 5730 años, calcula, en años cuando proceda:
a) La constante de desintegración del carbono-14.
b) La semivida del carbono-14.
c) El tiempo que tarda una muestra de carbono-14 en reducirse a la mitad.
d) El tiempo que tarda una muestra de carbono-14 en reducirse a la cuarta parte.
e) La edad que debe de tener una momia, sabiendo que ya solo queda un 40% del carbono-14 original.
f) La proporción de carbono-14 que quedará actualmente en la momia de un faraón que muriese hace 5000 años.Aplicando las fórmulas por orden, tenemos:
Y cabe comentar algunas cosas sobre los resultados. Las cuestiones b) y c) tienen el mismo resultado porque la c) pregunta, en esencia, por la semivida. La cuestión d) tiene como respuesta el doble de las anteriores porque si en 3970 años la muestra se reduce a la mitad, en el doble de tiempo se reducirá a la mitad de la mitad, es decir, una cuarta parte.
Como se puede apreciar, conocer la actividad radiactiva de los distintos elementos presentes en la Tierra puede servir para indicar la edad de sus fuentes, y afortunadamente disponemos de núcleos con vidas medias muy dispares para analizar grandes rangos de tiempo. Como el carbono-14 tiene una vida media de miles de años es útil para analizar restos de seres vivos que muriesen en un tiempo de ese orden de magnitud, pero por ejemplo el uranio ha resultado útil para estimar los 4,55 mil millones de años de la Tierra. A estas estimaciones se las denomina dataciones radiométricas.
El efecto túnel y la radiactividad permitieron el comienzo del análisis matemático de una rama de la ciencia que estaba a punto de nacer: la física nuclear. Y en el siguiente capítulo veremos cómo esta nos acercó a la comprensión de las estrellas, del origen del universo, y acabó facilitando el desarrollo del famoso modelo estándar de la física de partículas.
ACTIVIDAD RECOMENDADA
1. Argumenta la relación entre la tercera ley de la termodinámica, que establece que la temperatura cero es inalcanzable, y el principio de incertidumbre de Heisenberg.
2. Sabemos que la vida media de un neutrón suelto es de 886 s. Si tenemos una muestra de neutrones y sabemos que su actividad es de 500 bq, calcula:
a) La constante de desintegración del neutrón.
b) La cantidad de núcleos de neutrón en la muestra.
c) El tiempo que tardarán los neutrones en reducirse a la mitad.
d) La cantidad de neutrones que quedarán tras una hora.